近年来��
,我国儿童侵袭性真菌感染的发病率和病死率逐年上升��
,伏立康唑作为新一代三唑类广谱抗真菌药物��
,是治疗侵袭性曲霉病��
、对氟康唑耐药的念珠菌感染以及部分其他药物治疗无效的真菌病的一线用药��
。随着伏立康唑在儿童抗真菌感染领域的应用增多��
,对其不同给药方案的安全性和有效性评价成为研究热点[1]��
。
目前全球范围内对儿童伏立康唑治疗侵袭性真菌感染的给药方案尚无一致意见��
。2006年伏立康唑注册说明书中的儿童静脉给药方案与成人一致 ( 维持量每12小时1次��
,每次4mg·kg-1 ) [2]��
。2008年美国真菌病诊治指南指出: 为使儿童获得与成年 人静脉维持剂量的暴露量相当��
,儿童患者中的静脉维持剂量应当为7mg·kg-1每日2次[3]��
。2009年我国《儿童侵袭性肺部真菌感染诊治指南》中推荐的方案为: 7mg·kg-1每12小时1次静脉滴注或第1天6mg·kg-1每12小时1次��
,随后4mg·kg-1每12小时1次静脉滴注; 口服剂量: 体质量<40 kg��
,100 mg每12小时 1次; 体质量≥40 kg��
,200mg每12小时1次[4]��
。比较可发现��
,国内指南并未严格区分成人与儿童给药方案的不同�
。相关研究表明��
,在给予相同剂量伏立康唑后��
,体内血药浓度具有较大的个体变异��
,这给临床带来了挑战[5]��
。据国外文献报道�
,伏立康唑的安全浓度范围是1~5.5 μg·mL-1 ��
,当血药浓度低于1μg·mL-1可能引起治疗失效��
,当浓度高于5.5μg·mL-1 可能引起神经毒性和肝功能损伤[6-7]��
。
而我国目前尚无这方面的大样本研究报道��
。治疗药物浓度监测(TDM) 通常用于治疗浓度范围窄的药物��
,伏立康唑符合这一特点��
。因此�
,有必要进行伏立康唑的药物浓度监测��
,为合理制定我国儿童的伏立康唑用药方案提供研究数据��
,并提高儿童用药的安全性和有效性��
。
76例侵袭性真菌感染并接受伏立康唑治疗的患儿为研究对象��
。男性52例��
,女性24例��
。诊断标准参照欧洲癌症研究和治疗组织/侵袭性真菌感染协作组和美国国立变态反应和感染病研究院真菌病研究组共识组( EORTC /MSG) 发布的侵袭性真菌病修订定义( 2008年修订版)[8]��
,确诊20例��
,临床诊断21例��
,拟诊35例��
。
所有患儿接受伏立康唑静脉滴注和(或)口服进行的序贯疗法治疗��
。首次给药第一个24 h给予负荷剂量��
,每12小时给药1次�
,每次6mg·kg-1 静滴�
。随后给予维持剂量��
,每12小时给药1次��
,每次4mg· kg-1 静滴��
。由于口服片剂的生物利用度很高 ( 96% ) ��
,在有临床指针时予伏立康唑口服给药序贯治疗��
,每12小时给药 1次��
,每次4mg·kg-1 口服��
。并根据TDM结果和临床疗效调整后续给药剂量��
。患儿连续给药至少3d达稳态后��
,在下一次给药前采集静脉血��
,离心取上层血浆��
,进行药物浓度检测��
。每名患儿至少采集一次血样测定药物浓度��
。依据国外文献报道��
,伏立康唑目标浓度范围设定为 1~5.5μg·mL-1 ��
。
伏立康唑给药2~6周后符合以下条件患儿为治疗有效:
(1) 临床症状及体征明显减轻或消失(包括体温��
、肺部啰音和痰量) ;
(2) 影像学病灶明显吸收或消失;
(3) 真菌培养阳性转阴性�
。
✳不符合者视为治疗失败病例��
。
自76 名患儿共采集伏立康唑谷浓度检测血样 99 例��
,其中 92 例在静脉给药后采集��
,7例在口服给药后采集��
。静脉给药剂量中位值为5.85mg·kg-1·dose-1 (4.15~8.82mg· kg-1·dose-1 ) ��
,口服给药剂量中位值为5.38mg·kg-1·dose-1 (3.60~8.12 mg·kg-1 ·dose-1 ) (P=0.87) ��
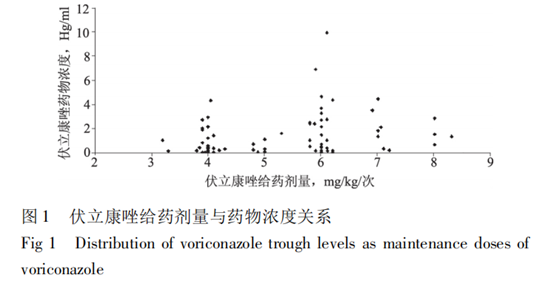
。测定伏立康唑浓度中位值为0.784 μg· mL-1 ( 0.025~9.910 μg·mL-1) ��
,其中44例 ( 44.4% ) 达到目标浓度范围(1~5.5 μg·mL-1) �
,53例(53.5% ) 浓度<1μg·mL-1��
,2例(2.02%) 浓度>5.5 μg·mL-1 ��
,见图 1��
。个体间和个体内血药浓度变异系数分别为97.0% 和69.6% ��
。给药剂量与血药浓度之间缺乏相关性(r= 0.252�
,P=0.315) ��
。
患儿平均年龄( 2.45 ± 3.22) 岁��
,分布2个 月~14 岁��
,6岁以下64 例 ( 84.2% ) ��
,6 岁~14 岁12 例( 15.8% ) ��
。年龄<6 岁的患儿与年龄 >6 岁的患者相比��
,谷浓度要达到设定范围( 1~5.5 μg·mL-1 ) 需要给予更高剂量的伏立康唑( 6.1 mg·kg - 1 /次 vs.4.55 mg·kg-1 /次��
,P<0.05) ��
,见图 2��
。

分析 41 例确诊( 20例) 和临床诊断( 21 例) 侵袭性真菌感染患儿的血药浓度( 共 60 份血样) 与临床疗效相关性��
,32 例患儿( 43 份血样) 临床治疗有效��
,9 例患儿( 17 份血样)
治疗失败��
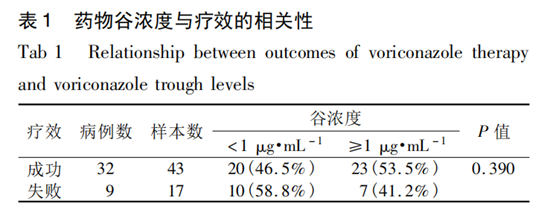
。治疗成功的患儿中��
,谷浓度< 1 μg· mL-1 的血样20 份( 46.5% ) ��
,谷浓度≥1 μg·mL-1 的血样 23 份( 53. 5% ) ; 治疗失败的患儿中��
,谷浓度<1μg·mL-1的血样 10 份( 58. 8% ) ��
,谷浓度≥1 μg· mL-1的血样7 份( 41. 2% ) ��
。可见谷浓度 < 1 μg· mL-1的样本中治疗失败率高于成功率( 58.8% VS 46.5% ) ��
,但差异无统计学意义( P = 0.390) ��
,见表1��
。5 名患儿治疗过程中监测谷浓度<1μg·mL-1 且疗效不佳��
,通过提高给药剂量使谷浓度达 1 μg· mL-1 以上��
,最终治疗有效��
。
2 例谷浓度≥5.5 μg·mL-1 的患儿均出现肝功能异常��
,而低于此浓度则无此不良反应发生; 1例患儿出现皮疹��
。上述不良反应于患儿停药后逐渐好转��
。
讨论��
:
据国外文献报道�
,伏立康唑推荐的目标治疗浓度范围是 1~5.5 μg·mL -1 ��
。选择1mg·L-1作为低限是考虑了以下因素: (1) 念珠菌属的 MCI��
,(2) 伏立康唑对念珠菌属 MCI 的拐点��
,(3) 对曲霉属MCI 的拐点��
。从以往的研究看��
,谷浓度≤1 μg·mL-1的 患者疗效不佳的比率更高��
。而当谷浓度超过5.5 mg ·L-1��
,患者可能出现神经系统毒性反应��
、视觉障碍��
、肝功能异常[6-7]��
。本研究中测定伏立康唑浓度的中位值为0.784 μg·mL-1 ( 0.025~9.910 μg·mL-1 ) ��
,其中仅 44 例( 44.4% ) 达到目标浓度范围( 1~5.5μg·mL-1 ) ��
,53 例( 53.5% ) 浓度 < 1 μg·mL-1 ��
。提示在目前常规给药方案下��
,部分患儿难以达到目标治疗浓度��
。2 例( 2.02% ) 谷浓度≥5. 5 μg·mL-1 的患儿均出现肝功能异常��
,而低于此浓度则无此不良反应发生��
,说明高血浆浓度的伏立康唑可引起肝脏毒性�
。而在谷浓度达到设定范围( 1~5.5 μg·mL-1 )的患儿中��
,年龄< 6 岁的患儿与年龄>6 岁的患者相比��
,伏立康唑的给药剂量更高( 6.1 mg·kg-1 /次VS 4.55 mg·kg-1 /次��
,P<0.05) ��
。说明低龄儿童较年长儿具有更高的药物清除能力和更大的分布容积��
,因此为达到治疗浓度需要给予更高剂量的伏立康唑[8]��
。
彩神vi生物伏立康唑血药浓度检测全自动化学发光解决方案
彩神vi生物始终坚持科技创新��
,关注儿童用药安全��
,彩神vi生物伏立康唑检测试剂盒(化学发光法)通过搭载全自动化学发光免疫分析仪��
,快速便捷准确检测伏立康唑血药浓度��
,为患者个体化治疗提供解决方案��
,关注儿童用药健康��
,彩神vi始终在行动�
!


参考文献
[1] Liao Y��
,Chen M��
,Hartmann T��
,et al. Epidemiology of opportunistic invasive fungal infections in China: review of literature [J]. Chinese medical journal��
,2013��
,126( 2) : 361-368.
[2] Leveque D�
,Nivoix Y��
,Jehl F��
,et al. Clinical pharmacokinetics of voriconazole [J]. International journal of antimicrobial agents��
, 2006��
,27( 4) : 274-284.
[3] Walsh TJ��
,Anaissie EJ��
,Denning DW��
,et al.Treatment of aspergillosis: clinical practice guidelines of the Infectious Diseases Society of America[J].Clinical infectious diseases: an official publication of the Infectious Diseases Society of America��
,2008��
,46 ( 3) : 327-360.
[4] 中华医学会儿科学分会呼吸学组编辑委员. 儿童侵袭性肺部真菌感染诊治指南( 2009 版) [J]. 中华医学信息导报�
,2009��
, 24( 2) : 21-22.
[5] Karlsson MO��
,Lutsar I��
,Milligan PA. Population pharmacokinetic analysis of voriconazole plasma concentration data from pediatric studies[J]. Antimicrobial agents and chemotherapy��
,2009��
,53 ( 3) : 935-944.
[6] Dolton MJ��
,Ray JE�
,Chen SC��
,et al. Multicenter study of voriconazole pharmacokinetics and therapeutic drug monitoring[J]. Antimicrobial agents and chemotherapy��
,2012��
,56( 9) : 4793-4799.
[7] Pascual A��
,Calandra T��
,Bolay S��
,et al.Voriconazole therapeutic drug monitoring in patients with invasive mycoses improves efficacy and safety outcomes[J]. Clinical infectious diseases : an official publication of the Infectious Diseases Society of America��
,2008��
, 46( 2) : 201-211.
[8][1]吴婷婷,张杨,刘玲玲,刘艳,徐三清.儿童伏立康唑治疗药物浓度监测的临床意义[J].中国医院药学杂志,2017,37(23):2387-2390.DOI:10.13286/j.cnki.chinhosppharmacyj.2017.23.18.